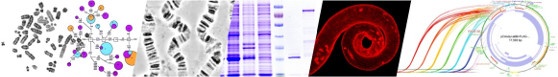
Будущий Институт молекулярной и клеточной биологии СО РАН: главная цель - преодолеть отставание
Сайт Сибирского отделения РАН COPAH.info 30 июня 2010 г.
Недавно Председатель Сибирского отделения РАН академик А.Л.Асеев сообщил о перспективе открытия в составе СО РАН трех новых институтов, в том числе – Института молекулярной и клеточной биологии в Новосибирском научном центре. У истоков идеи его создания стоит академик Игорь Фёдорович Жимулёв, ответивший на вопросы COPAH.info

В Новосибирске уже работают два института СО РАН относительно близкого профиля. С чем связана необходимость создания третьего, в чем будет его научная специфика?
Почему возникла необходимость создания именно такого института? Потому что действующие институты биологического профиля не покрывают всей новой фундаментальной проблематики, появившейся и развивающейся сегодня в сфере наук о жизни. Институт цитологии и генетики, как следует из его названия, и занимается цитологией и генетикой. Генетика – это все-таки наука о связи какого-то конкретного признака и конкретного гена. Высокого уровня Институт химической биологии и фундаментальной медицины имеет зримый химический, биохимический профиль с выходом на медицину, в том числе и практическую. А молекулярная и клеточная биология, о которой мы говорим, это, фактически, новая наука, которая является синтетической. В ней используются физические, химические методы, а главное – множество методов, разработанных внутри самой этой науки. Смысл всех этих методов – в том, чтобы заставить работать клетку саму на себя. За последние 30 лет произошел синтез генетических исследований на разных объектах. Например, в частной генетике дрожжей находят активаторы транскрипции (по-простому «включатели активности генов»), система взаимодействия "белок-ген". Если перенести такую систему в геном, скажем, дрозофилы, то она, как объект, приобретает огромные новые возможности. Или у бактерий некоторые белки, полученные в результате работы генов, создают нерастворимый в воде осадок, да еще окрашенный. При их включении в любом геноме по этой окраске можно судить о работе определенного гена (это так называемые гены-репортёры). При этом мы ограничиваемся только пересадкой тех или иных элементов и не вмешиваемся в деятельность клетки: вся прелесть в том, что клетка работает сама, да и сам перенос произошел поколение назад. Этот метод, называемый трансгенезом – одна из важнейших основ молекулярно- клеточной биологии.
За открытие маркёров трансгенеза с помощью флуоресцирующих белков полтора года назад была присуждена Нобелевская премия. Возникла целая палитра методов чисто генных манипуляций с клетками различных модельных организмов, от червя до человека, при единственном первоначальном вмешательстве – трансгенезе.
При создании трансгенных конструкций появилась возможность строить заранее спланированные схемы генных изменений, чего в биологии никогда не было.
Для наглядности сравню это с текстом, например, стихотворным – упорядоченным согласно определенному алгоритму. Мы – с точностью до буквы, до знака! – вырезаем необходимый нам отрезок этого текста и вставляем в другой. То, что в компьютере будет командами вроде "копировать-вставить", на практике будет осуществлено, например, специальными ферментами рестрикции. Молекулярную "вырезку" для переноса генов необходимо ввести в вектор. Одноименное НПО не зря так называется. Вектор на языке нашей науки – это переносчик. Сотрудники одной из наших лабораторий сегодня создают изумительные векторы: он сам встраивается, при воздействии на различные регуляторные фрагменты простыми факторами, например, нужной температурой, можно включать требуемые гены, вы можете играть на процессах включения гена, как на пианино. И в результате мы получаем не просто второй "текст" со фрагментами первого, а единую структуру нового гена, монолитную и гармоничную. Это тонкая молекулярная работа, требующая особой степени умения учёных, чистоты – посуды, приборов, всего остального, особой точности дозировок. 20 лет назад это было тяжелейшим трудом, теперь эту работу выполняют даже наши студенты и аспиранты.
Сначала, в середине 1970-х годов такие работы проводились в интересах клонирования – создания молекул, генов клеток или организмов с одинаковыми признаками, организмов - клонов. Затем появился целый класс задач, как фундаментальных, так и прикладных. В целом, они сводятся к тому, чтобы клетка видоизменялась и работала под контролем человека. Надо сказать, что мы в этом направлении сильно отстаем – прежде всего, от США и Европы.
Сегодня в СМИ мы читаем все больше и больше предостережений о жутковатых последствиях, к которым могут привести манипуляции с генными структурами…
Фантастов, надо сказать, у нас всегда было много. Частично их предсказания сбываются: тот же "Гиперболоид инженера Гарина" воплотился в лазер, в том числе и боевой. Но мировой катастрофы это не принесло. Точно так же и атомное оружие, примененное дважды в мировой истории, не погубило человечество, зато атомные проекты послужили мощным толчком для развития многих направлений науки. Новые явления научно-технического прогресса при их рождении зачастую демонизируют, но вопрос только в контроле. Какое общество – такой и контроль. Приведу пример с использованием стволовых клеток: от полного запрета маятник качнулся к бесконтрольности, и в Москве множество фирм предлагают услуги по их пересадке. Не следует только попадаться на их удочки.
Не нужно пугаться явлений, не понимая их смысла. Например, "генные модификации". На самом деле человечество использует их тысяч пять, думаю, лет – с того момента, как люди начали осознанно выводить сорта растений и породы животных.
Вся селекция – это процесс генных модификаций, просто гены переносятся самым простым методом, скрещиванием. В чем величие Вавилова? Он нашел принципы подбора исходного материала для селекции и предсказывал возможности его модификаций на основе закона гомологических рядов. Вавилов также выявил регионы поиска исходных образцов и создал богатейшую коллекцию – около 300.000 образцов семян. Насколько велико значение этой коллекции свидетельствует такой факт: в годы Великой Отечественной войны немцы захватили опытные поля ВИРа (Всесоюзного института растениеводства), вырастили растения, подчистую обмолотили и увезли образцы семян в Германию. Прихватили и всю документацию. А в блокадном Ленинграде многие сотрудники ВИРа, ученики Вавилова, умерли от голода, но не дали ни людям, ни крысам тронуть тонны коллекционного семенного материала, фактически зерна, которое позволило бы им выжить.
Как Вы оцениваете состояние сегодняшних российских, в частности, сибирских исследований в области клеточной и молекулярной биологии? Как они выглядят по сравнению с зарубежными?
Молекулярная и клеточная биология - ведущая в настоящее время наука о жизни. Недаром программа академика РАН Георгия Павловича Георгиева, с открытым письмом в защиту которой выступили 119 видных российских ученых, так и называется. Половина всех затрат на науку в мире приходится на молекулярную и клеточную биологию. Начало крупным инвестициям в эту отрасль знаний положил Рональд Рейган. Поэтому США быстро ушли вперед, а в нашей стране как раз в 1990-е произошел развал научных структур, и мы существенно отстали. Наша задача – быстро возрождать это направление. Что есть у нас в Сибирском отделении сегодня? Хорошие заделы по геномике, есть оборудование, математические программы, а главное – люди. У нас – в сегодняшнем отделе ИХБиФМ - есть признанные специалисты международного уровня по сравнительной геномике, например, профессор Александр Сергеевич Графодатский. Сейчас в мире под руководством американцев запускается амбициозный "Проект Genome 10K" по расшифровке геномов 10.000 биологических видов одновременно. Графодатский был сначала единственным исследователем из Евразии, приглашенным в эту программу – потом, правда, добавилось еще пять. Его сотрудники работают в Англии, Швейцарии, других странах мира. Есть у нас маленькая лаборатория молекулярной генетики человека, руководит ей Рэм Израилевич Сукерник. Там всего 4 научных сотрудника, но занимаются они очень важной тематикой – митохондриальными ДНК. У такой ДНК человека всего 16.000 пар нуклеотидов, тогда как полный клеточный набор достигает 3 миллиардов. Они эволюционируют быстрее других ДНК, а главное – являются стабильным маркером ряда признаков, передаваясь от поколения в поколение по материнской линии без рекомбинации.
По митохондриальной ДНК, в частности, подтвердили принадлежность найденных на Урале останков членов царской семьи, а группа немецких исследователей во главе со Сванте Паабо определила ранее неизвестный вид гоминида, существовавшего параллельно с неандертальцем ("Человек Алтайский").
По этой ДНК ученые прослеживают происхождение и распространение Homo sapiens по земному шару, добиваются многих результатов в палеоантропологии, археологии, этнографии. Очень интересны исследования митохондриальной ДНК и для криминалистики – в плане идентификации личности. А прежде всего – для медицины, поскольку за многие наследственные болезни отвечает именно она. Например, болезнь Лeбера, когда человек, прожив лет до 30, стремительно слепнет из-за отмирания зрительного нерва вследствие мутации в митохондриальной ДНК.
Не так давно открыли некодирующие микро-РНК. Таким образом, найден новый вид контроля клеточных и молекулярных процессов с их помощью: эти микро-РНК контролируют формирование продуктов генов и зачастую служат гарантами нормального наследственного развития организма. У нас несколько человек занимаются этой проблематикой, важной с точки зрения медицинской диагностики – например, онкологических заболеваний, в частности доктор наук Николай Николаевич Колесников. Ведь рак – это даже не заболевание, а процесс изменения скорости деления клеток с нормального на патологически быстрое. В нашем отделе лаборатория из 5 человек занимается как раз проблемами генетического контроля за процессами клеточного деления. Скажу еще об одном направлении – исследованиях на политенных хромосомах, здесь мы, без ложной скромности, занимаем лидирующие позиции в мире, у меня самого вышла трёхтомная монография в США об этом типе хромосом.
Ваш отдел чем-то похож на так называемый "кадрированный полк", состоящий из командиров экстра-классса, который может быть развернут в боеготовое формирование, как только туда поступят обученные солдаты…
"Солдат", как раз, не должно быть много, должны быть квалифицированные исследователи. У нас в отделе около 100 человек, из них 65 научных сотрудников, остальные – студенты, аспиранты, технический персонал. Около 50 имеют ученую степень, три лауреата Государственной премии. У нас сегодня почти нет лаборантов – 12 на отдел из ста человек. Когда-то я работал в Англии, в лаборатории будущего нобелевского лауреата Тима Ханта, то видел, на что способны лаборанты высшей квалификации. В наших же условиях мало кто доверит лаборанту подготовку растворов – лучше сам сделает. В основном, работает молодежь – работников моложе 35 лет тоже более половины. Среди них по 5-6 лауреатов золотых медалей Европейской Академии и РАН для молодых учёных.
Слово "институт" подсознательно ассоциируется с отдельным зданием или даже комплексом. Насколько новому институту необходимы новые стены?
Если нам дадут новый корпус, строящийся около ИХБиФМ, то хорошо. Если не дадут – стройка не самоцель, останемся, где сидим. Все здания и сооружения находятся в распоряжении Сибирского отделения, руководство которого, я надеюсь, найдет оптимальное решение.
В Концепции развития СО РАН до 2025 года численность будущего института к 2020 году определена в 300 человек. Я бы создавал его в два этапа. На первом – принял бы в существующий наш отдел ИХБиФМ еще 50 человек из Института цитологии и генетики, которые уже изъявили желание работать у нас. Тогда численность достигла бы половины планируемой. А вторым этапом стало бы расширение до заданной численности за счет тех маленьких лабораторий, которым необходим кадровый и материальный рост, а также создание новых лабораторий. Та же четверка сотрудников, занятая проблемами митохондриальных ДНК, должна стать полноценной лабораторией. Или взять доктора биологических наук Александра Васильевича Вершинина – он девять лет проработал в Англии, крупнейший специалист по теломерам, концевым участкам хромосом. Полгода назад по этой теме была присуждена Нобелевская премия, кстати, моей знакомой, Элизабет Блэкберн. Вершинин – организатор симпозиумов по теломерам, его постоянно приглашают на международные конференции. Это прекрасный специалист, но он фактически один – таким, как Вершинин, нужны молодые сотрудники, нужна материальная база. Тоже, по вашему сравнению, "кадрированный полк". Аналогичные доводы можно приести по отношению к лабораториям В.В. Соколова, Л.В. Омельянчука, С. А. Демакова. Рядом со мной работает совсем молодой исследователь, Степан Белякин, он возглавил группу геномно-протеомной направленности, ее тоже необходимо расширять. Тем более, что они сегодня работают с микрочиповыми технологиями, причем очень успешно - в качестве критерия назову их статьи в PNАS (Труды американской академии наук) или в СELL с самым высоким в нашей области импакт-фактором. Есть в составе отдела и прекрасно отлаженная и работающая лаборатория иммуногенетики во главе с профессором А.В. Тараниным. Это как пример.
Каким должен быть первый шаг в создании нового института?
Первое необходимое официальное событие в цепочке принятия решений – это конкретное решение Президиума СО РАН. Потом таких важнейших решений будет тоже много, но это - главное. Но и сегодня мы не сидим сложа руки. При нашем отделе уже создан свой ученый совет, совет молодых учёных, свой семинар, начато проведение международных конференций, получена лицензия на обучение в аспирантуре. Формальность, конечно, но у многих институтов ее нет. Мы обратились в ВАК, чтобы наш совет стал диссертационным по молекулярной генетике и клеточной биологии – процесс идет медленно, но идет. Добавлю еще, что у членов нашего ученого совета высокие индексы цитирования: у пятерых свыше 1000. Это, надо полагать, признанный показатель научного авторитета.
Мы хотели бы формировать новый институт по схеме Лаврентьева – сочетая фундаментальную науку, науку прикладную и образование. Не дожидаясь каких-либо реорганизаций, нам надо разрабатывать выходы в практику.
Здесь все должно быть сосредоточено, в конце концов, на человеке, на его здоровье и долголетии. И нужно создавать в университете свою кафедру. У нас, как было сказано, молодые сотрудники, но о преемственности следует думать заранее. Если говорить о научной стратегии на десятилетия вперед, то сегодня она предполагается в области полных геномных, а потом – и протеомных исследований, на том, как вся эта наследственная информация уложена в составе хроматина и хромосом, и как эта укладка обеспечивает возможности функционирования этой информации. Если мы получим необходимые возможности, то у нас будут все возможности преодолеть отставание от наших западных коллег.
Беседовал Андрей Соболевский