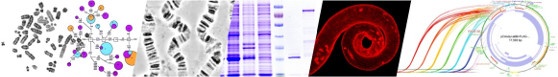
На "Технопроме-2018" рассказали о клеточных технологиях для лечения рака
Сайт Наука в Сибири 29 августа 2018 г.
Газета Наука в Сибири №33 от 30 августа 2018 г.
Сайт Российской Академии наук 29 августа 2018 г.
Медицинский информационный портал SIBMEDA 29 августа 2018 г.
Сайт Новости Новосибирской области VN.RU 29 августа 2018 г.
Разработки сибирских ученых в области клеточных технологий могут использоваться для лечения онкологии с эффективностью 70-90 %. Речь идет о CAR-T терапии, когда пациенту вводятся собственные Т-лимфоциты с присоединенным химерным рецептором, который одним концом распознает опухолевые клетки, а другим активирует лимфоциты. CAR-T клетка уничтожает опухолевые образования и делится, работая до тех пор, пока есть онкомишени.
“В лаборатории иммуногенетики Института молекулярной и клеточной биологии СО РАН получено более 100 вариантов конструкций, кодирующих CAR (лимфоциты с химерными рецепторами. — Прим. ред). При этом у нас есть как оригинальные разработки, так и аналогичные зарубежным, наш коллектив обладает всеми компетенциями для производства CAR-T клеточных продуктов. Сейчас ведутся исследования их эффективности на мышиных моделях. Мы могли бы приступить к лечению пациентов терминальной стадии онкологических заболеваний в ближайшие время, например в течение полугода. Вопрос только в том, когда можно будет реально это делать в рамках действующего законодательства. Пока в нем нет соответствующих нормативов”, — рассказал старший научный сотрудник лаборатории иммуногенетики ИМКБ СО РАН кандидат биологических наук Сергей Викторович Кулемзин, выступая на технологическом треке “Биотехнологии и геномные технологии” на VI Международном форуме и выставке технологического развития “Технопром-2018”.
В сентябре 2017 года управление по контролю за качеством пищевых продуктов и лекарственных препаратов США FDA одобрило препарат Kymriah на основе CAR-T технологии против острой лейкемии хронического лейкоза. В Китае занимаются лечением пациентов терминальной стадии на этапе клинических испытаний CAR-T продуктов. В России Федеральный закон № 180 “О биомедицинских клеточных продуктах” требует длительных исследований подобных препаратов, прежде чем они будут выпущены на рынок.
“В западной практике путь от появления клеточного продукта в лаборатории, его проверки на мышах и использования у пациентов часто очень короткий. При уверенных положительных результатах на мышиных моделях сразу переходят к терапии уже на людях. Отличие клеточных продуктов от классических препаратов заключается в том, что носителем эффекторной функции является собственная клетка человека, и огромное количество вопросов, связанных с безопасностью лекарственного средства, отпадает. Однако если утверждать препараты клеточной терапии так, как предписывает Федеральный закон (аналогично химическим препаратам. — Прим. ред), то технология никогда не будет работать на полную мощность, — отметил Сергей Кулемзин. В нашей стране в применении методов CAR-T терапии для лечения раковых заболеваний заинтересованы и медицинские центры, и пациенты, есть соответствующая научная база.
“В России необходимо создание комбинированных CAR-T центров, в которых проводились бы одновременно фундаментальные исследования, создавались готовые клеточные продукты и там же проходили лечение пациенты. Только таким образом, собрав все стадии в одном месте, можно эффективно, “на лету” применять и оптимизировать CAR-T клеточную терапию”, — добавил Сергей Кулемзин.
PDF-файл статьи